Introducción
Se estima que aproximadamente el 40% de los linfomas presentan manifestaciones extranodales, es decir, fuera de los ganglios linfáticos y del anillo linfático parafaríngeo, con posible compromiso de cualquier órgano del cuerpo1,2.
El compromiso del peritoneo por el linfoma se denomina linfomatosis peritoneal (LP) y tiene baja frecuencia de presentación (menos del 20% de los hallazgos extraganglionares), siendo más habitual su presencia asociada a los linfomas no Hodgkin agresivos3,4.
Debido a su baja incidencia, pocas veces es considerada como una posibilidad, y cuando se presenta, en general es confundida con un cuadro de carcinomatosis peritoneal por la similitud de sus hallazgos en las imágenes3.
La LP se acompaña de un deterioro progresivo en las condiciones del paciente, siendo de suma importancia su sospecha para iniciar un tratamiento óptimo, temprano y dirigido, cumpliendo las imágenes un rol fundamental en su sospecha diagnóstica inicial5.
La evaluación con mayor rédito para la estadificación y el monitoreo de la respuesta al tratamiento del paciente con linfoma es la tomografía computada por emisión de positrones (PET-TC) con 18F-fluorodesoxiglucosa (18F-FDG), que ofrece las características distintivas para el diagnóstico de esta afección poco frecuente6.
El propósito de este trabajo es realizar una revisión sobre la LP y la utilidad de la PET-TC para su diagnóstico.
Desarrollo
El peritoneo no contiene tejido linfoideo, motivo por el cual resulta infrecuente su compromiso en las enfermedades linfoproliferativas. No obstante, algunos linfomas, en general los no Hodgkin agresivos de alto grado, como el linfoma difuso de células B y el linfoma de Burkitt, entre otros, pueden manifestarse con diseminación peritoneal, lo que se conoce como LP3,4,7. Se cree que la diseminación peritoneal tiene diferentes vías, como a través de la superficie peritoneal visceral, el ligamento gastrocólico y el mesocolon transverso5,8.
El compromiso extranodal en los linfomas puede observarse prácticamente en cualquier órgano y tejido, mencionándose en orden decreciente de frecuencia como afectación extraganglionar el bazo, el hígado, el tracto gastrointestinal, el páncreas, la pared abdominal, el tracto genitourinario, las adrenales, la cavidad peritoneal y la vía biliar1,9.
Los primeros casos de LP se reportaron en torno a 1986 y fueron descubiertos en tres autopsias de pacientes con linfoma de alto grado10. Desde entonces se han reportado casos variados de LP, asociados en general a linfomas agresivos, aunque también se han descrito algunos en linfomas de bajo grado, siendo extremadamente infrecuente la LP en casos de linfoma de Hodgkin4,11.
Si bien la incidencia de la LP resulta incierta, se estima que sucede en menos del 20% de los casos de compromiso extranodal de los linfomas12. No obstante, algunos autores refieren un compromiso aún menos frecuente de la LP, la cual no superaría el 8% del compromiso extraganglionar en el linfoma13.
No existen unas características demográficas definidas predisponentes para desarrollar LP, aunque se describe mayor frecuencia en el sexo masculino y en pacientes de mayor edad13. El caso más joven reportado hasta la fecha fue un niño de 3 años, y hay publicados aislados casos en la adolescencia14,15.
La presentación clínica de los pacientes con LP es variable e inespecífica, en la mayoría de los casos con dolor abdominal, distensión, repercusión general y pérdida de peso5,16,17.
La LP puede ser la forma inicial de manifestación del linfoma, pero es más frecuente que se presente como evolución en el curso de la enfermedad linfoproliferativa, o incluso ser una expresión de la transformación de un linfoma indolente a uno de mayor agresividad11,18.
En la mayoría de los casos, la LP se acompaña de empeoramiento en las condiciones clínicas del paciente con linfoma, motivo por el cual resulta fundamental su diagnóstico temprano, tomando las imágenes un rol protagónico en su sospecha17.
En el pasado, la TC con contraste endovenoso era considerada el método de elección para la evaluación del paciente con linfoma en sus diferentes formas de presentación. Sin embargo, tiene sensibilidad limitada para detectar el compromiso linfomatoso de los ganglios de tamaño conservado, así como la afección de la médula ósea, del bazo y de los tejidos extranodales6,18.
El método de fusión PET-TC, gracias a ser un método híbrido, brinda información tanto morfológica (TC) como metabólica de las lesiones (PET), permitiendo diferenciar sitios fisiológicos y patológicos que presenten aumento de consumo del radioisótopo19,20. Por estos motivos, la PET-TC con 18F-FDG es en la actualidad el método de imágenes con mayor rédito para la estadificación, el seguimiento y el monitoreo de la respuesta al tratamiento del paciente con linfoma. Permite detectar tempranamente la eventual recurrencia de la enfermedad, así como confirmar las adenopatías residuales no activas y la fibrosis residual, y elegir sitios de biopsia incluso no accesibles, pero metabólicamente activos, aumentando con ello la probabilidad de un resultado diagnóstico11,19,21–23.
Si bien pueden existir mínimas discrepancias entre los centros para la realización del estudio de PET-TC en la evaluación del paciente con linfoma, la técnica habitual para su realización consiste en la inyección en una vena periférica de 0,08 mCi/kg de peso (300 MBq) de 18F-FDG, y a los 60 minutos de la inyección se adquiere primero una TC de baja dosis (130 kV 10 mGy, 966 DLP, 80 mA modulado) desde la base del cráneo hasta el tercio medio del muslo, sin contraste oral ni endovenoso, con respiración habitual suave, sin instrucciones de respiración contenida. Luego se realiza un escaneo PET superpuesto al mismo rango tomográfico realizado, sin cambiar la posición del paciente, adquiriendo camillas de 8 cm de longitud, de aproximadamente 90 segundos cada una.
La LP se caracteriza en las imágenes por presentar engrosamiento de la superficie peritoneal y del omento mayor, con nódulos multifocales dispersos por ella, con o sin líquido libre abdominal, simulando estos hallazgos un cuadro de carcinomatosis peritoneal5,7,11,24 (Fig. 1). Los mecanismos básicos para presentar asociación con ascitis se fundamentan en la obstrucción linfática que incrementa la permeabilidad de los vasos peritoneales y el consiguiente líquido libre abdominal25.
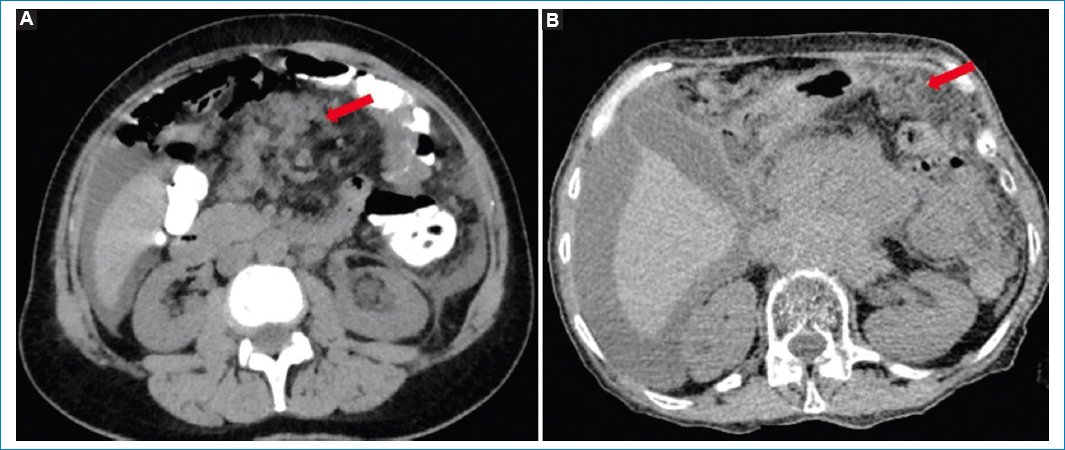
Figura 1. TC sin contraste endovenoso en imágenes axiales que evidencian engrosamiento peritoneal y del omento mayor (flechas), con nódulos dispersos y líquido libre abdominal. (A) Carcinomatosis peritoneal. (B) LP. Nótese la similitud de los hallazgos.
Los diagnósticos diferenciales de la LP a considerar en estos casos deben incluir no solo la carcinomatosis peritoneal, proveniente principalmente de patología primaria del ovario, gastrointestinal o de la mama, sino también las peritonitis de causa inflamatoria-infecciosa (como la tuberculosa), la patología orgánica primaria del peritoneo (mesotelioma) e incluso patologías menos frecuentes, como el pseudomixoma peritoneal y la sarcomatosis peritoneal, entre otras24,26,27.
Pensar en la LP como posibilidad es una condición desafiante para los radiólogos ya que, como se mencionó, muchas otras neoplasias peritoneales primarias y secundarias tienen hallazgos por imágenes similares, y en general puede ser confundida con la carcinomatosis peritoneal si no se la conoce12. Incluso, se han reportado casos de LP en pacientes con antecedentes oncológicos, que dificultan aún más y retrasan el diagnóstico de LP28.
Existen algunos hallazgos asociados a los mencionados que deben inclinar la sospecha diagnóstica hacia la LP, como la presencia de adenomegalias múltiples y en diferentes niveles, nódulos peritoneales más grandes que en la carcinomatosis (en general masas), compromiso de la raíz del mesenterio y del intestino delgado, y esplenomegalia11,29–31 (Figs. 2 y 3).
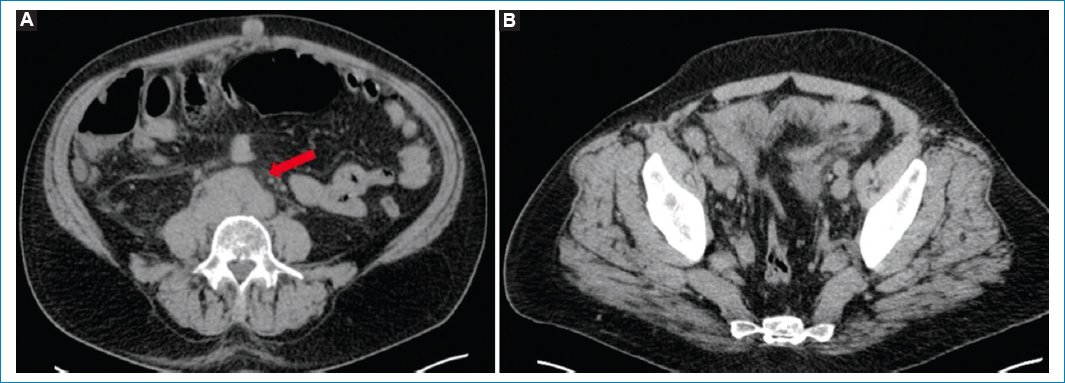
Figura 2. TC sin contraste endovenoso en un caso de LP, con hallazgos que respaldan la sospecha del diagnóstico. Nótense las adenomegalias retroperitoneales y pelvianas (flecha en A), los nódulos peritoneales múltiples y el grosero engrosamiento peritoneal (B).
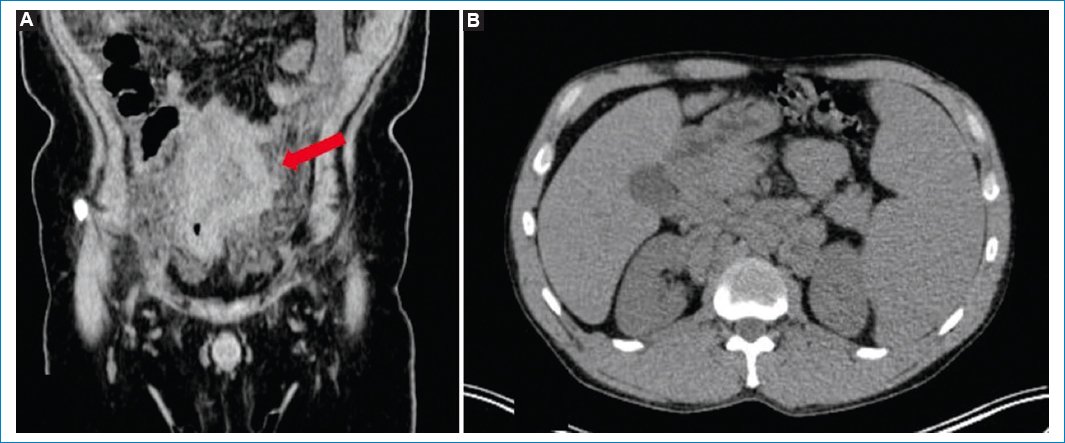
Figura 3. TC sin contraste endovenoso en un caso de LP, con hallazgos que apoyan la sospecha del diagnóstico. Compromiso del intestino delgado evidente en la imagen coronal (flecha en A) y esplenomegalia asociada (B).
Debido a que la PET-TC con 18F-FDG es el método de elección en la actualidad para la evaluación del paciente con linfoma, resulta fundamental conocer las características distintivas de la LP por esta técnica6,32.
Existen dos patrones respecto al metabolismo de la glucosa en la PET-TC para el diagnóstico de LP11:
- –Un patrón nodular, donde el hipermetabolismo se observa en relación con las masas y los nódulos peritoneales (Figs. 4–7)
- –Un patrón difuso, con avidez por la 18F-FDG en forma difusa por el omento mayor y la superficie peritoneal (Figs. 8–11)
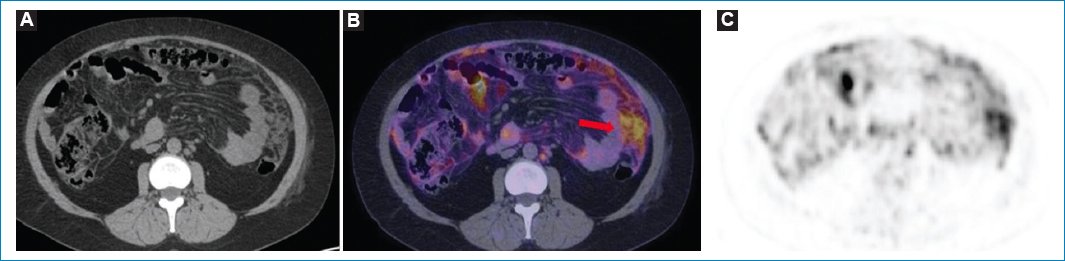
Figura 4. Mujer de 49 años con diagnóstico de linfoma no Hodgkin y LP. TC sin contraste endovenoso en imagen axial (A) que muestra patrón de engrosamiento nodular del peritoneo y adenopatías retroperitoneales. Fusión PET-TC (B) y MIP (C), cortes axiales, que demuestran el hipermetabolismo de los nódulos peritoneales y de las imágenes ganglionares (flecha).
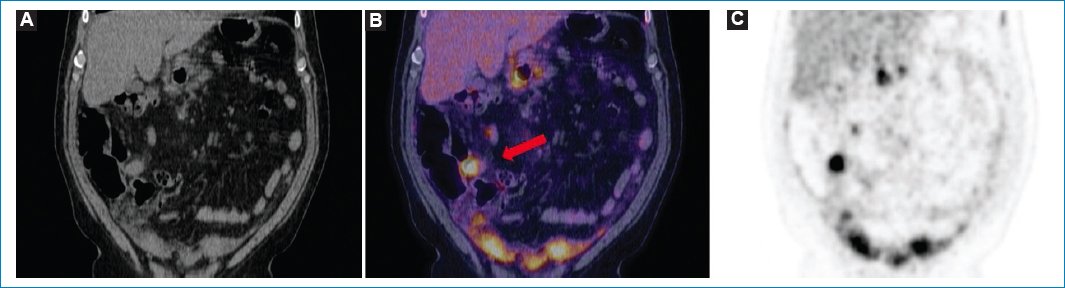
Figura 5. Paciente con diagnóstico de linfoma no Hodgkin y LP. Imágenes coronales de TC (A), fusión PET-TC (B) y MIP (C), en las que se objetiva el compromiso nodular hipermetabólico del peritoneo (flecha).
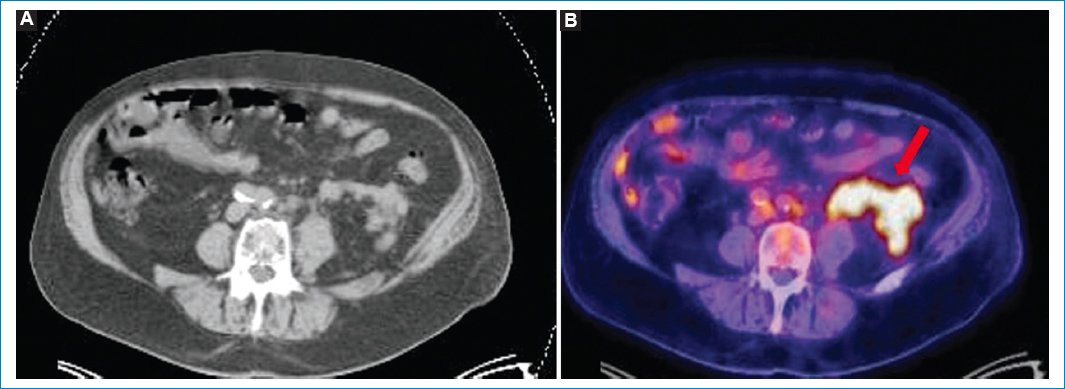
Figura 6. Varón de 74 años con diagnóstico de linfoma no Hodgkin difuso de células B en recaída, con LP. Imágenes axiales de TC (A) y fusión PET-TC (B) que evidencian engrosamiento nodular del peritoneo y de la fascia pararrenal anterior, con aumento de consumo de 18F-FDG (flecha).
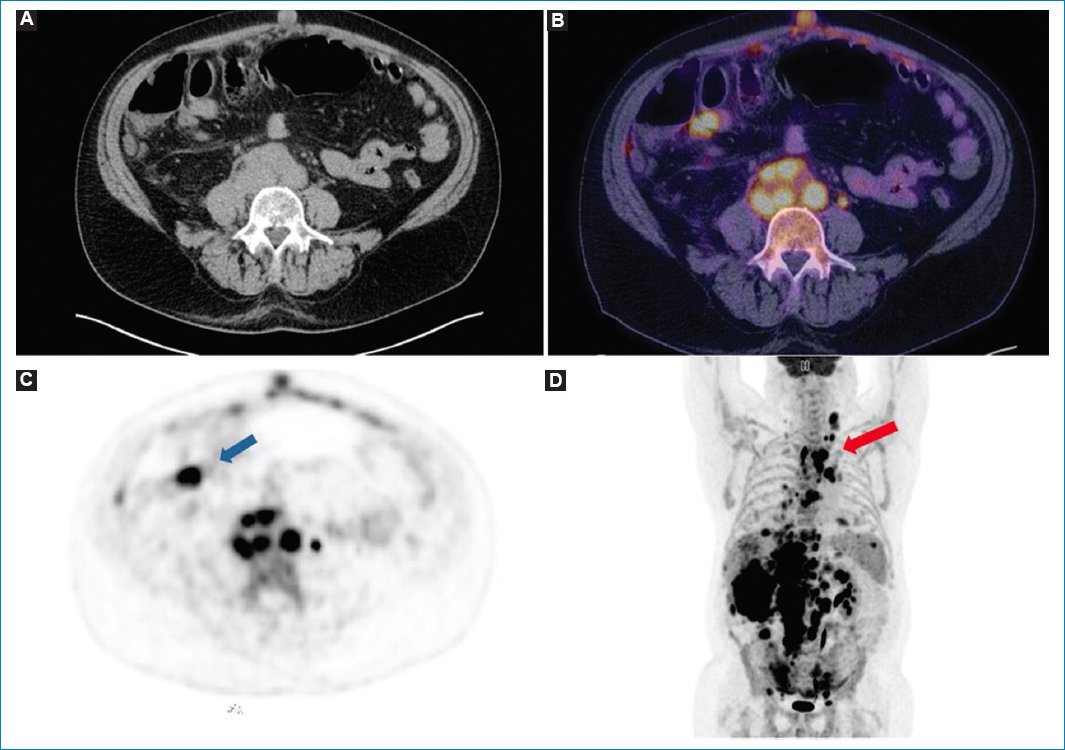
Figura 7. Varón de 65 años con diagnóstico de linfoma difuso de células B grandes y LP. Imágenes de TC (A), fusión PET-TC (B) y MIP (C y D) en las que se puede observar el patrón nodular hipermetabólico del peritoneo (flecha azul) y las adenomegalias en múltiples lugares (flecha roja).
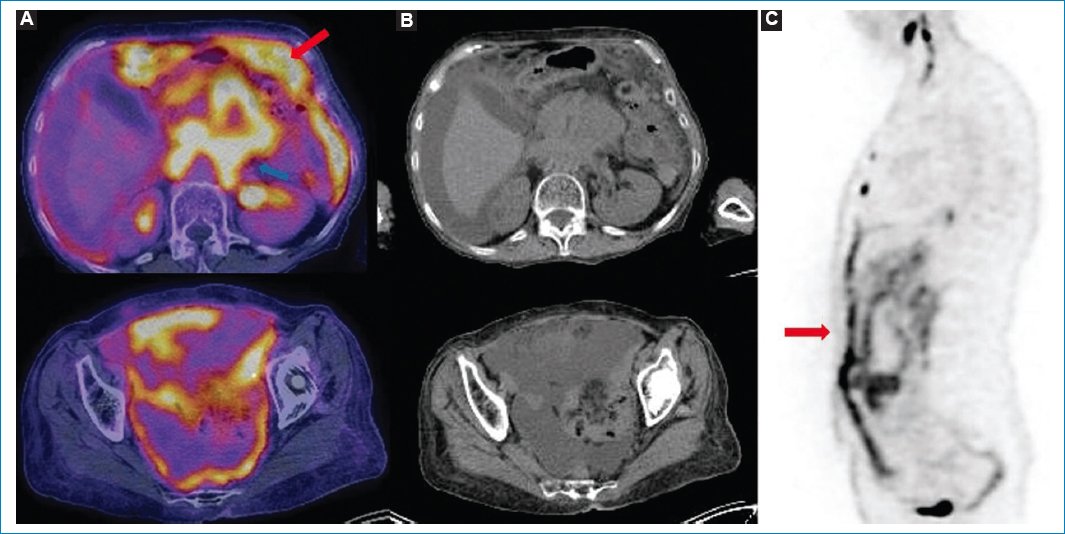
Figura 8. Varón de 71 años con linfoma difuso de células B de reciente diagnóstico, con LP, la cual presenta un patrón difuso de compromiso peritoneal (flecha roja), con adenomegalias hipermetabólicas (flecha azul) y líquido libre abdominal. Imágenes axiales de fusión PET-TC (A), TC (B) y corte sagital en MIP (C).
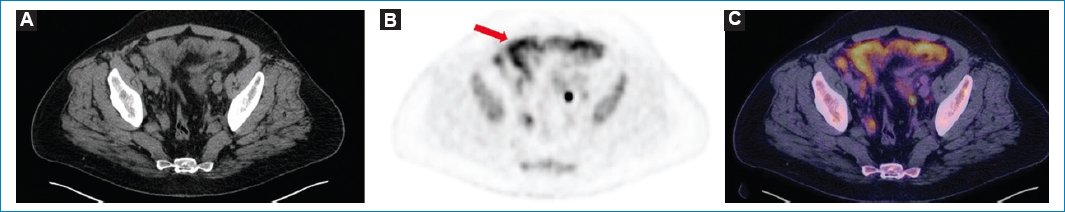
Figura 9. Paciente con diagnóstico de linfoma no Hodgkin e infiltración linfomatosa hipermetabólica difusa del peritoneo (flecha), evidente en las imágenes axiales de TC (A), MIP de PET (B) y fusión PET-TC (C).
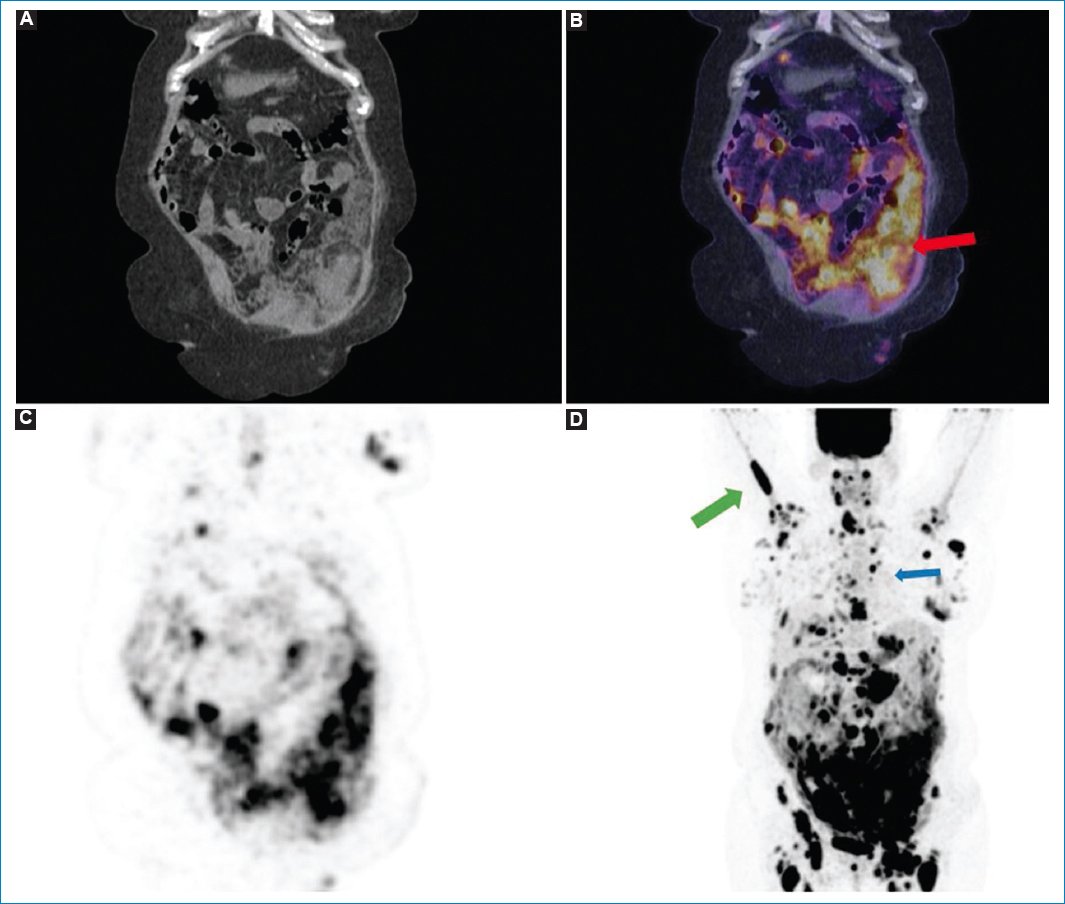
Figura 10. Mujer de 49 años con diagnóstico de linfoma no Hodgkin agresivo (misma paciente de la figura 4), con progresión de su enfermedad y de la LP, con actual compromiso difuso del peritoneo (flecha roja), adenomegalias múltiples hipermetabólicas en diferentes niveles ganglionares (flecha azul) y compromiso óseo (flecha verde); hallazgos evidentes en los cortes coronales de TC (A), fusión PET-TC (B) y MIP (C y D).
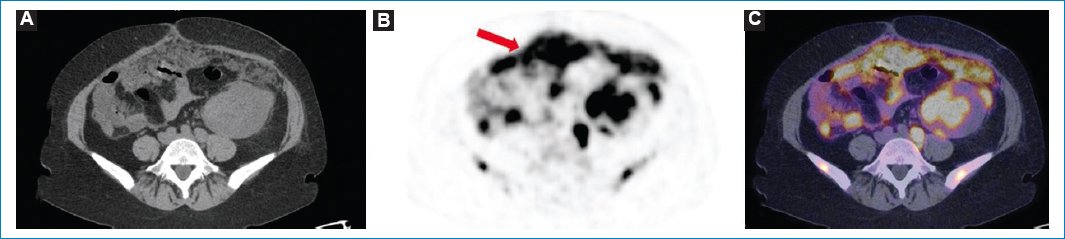
Figura 11. Varón de 66 años con diagnóstico de linfoma difuso de células B grandes y LP. Imágenes axiales de TC (A), MIP (B) y fusión PET-TC (C) que evidencian compromiso peritoneal difuso con aumento de consumo de 18F-FDG (flecha). Nótense, asimismo, las adenomegalias hipermetabólicas y las masas peritoneales acompañando el proceso difuso.
Estos patrones de LP en la PET-TC se acompañan en general de adenomegalias hipermetabólicas múltiples en diferentes sitios, así como de hipermetabolismo esplénico y de la médula ósea, colaborando para el diagnóstico certero y diferencial con las demás afecciones mencionadas (Figs. 12 y 13). Es importante recordar que la avidez de la 18F-FDG varía según el tipo de linfoma involucrado. Así, los linfomas de alta agresividad presentarán mayor metabolismo glucídico que aquellos linfomas indolentes o de bajo grado, variando también su avidez según el grado de respuesta a la quimioterapia instaurada6,19,21 (Fig. 14).
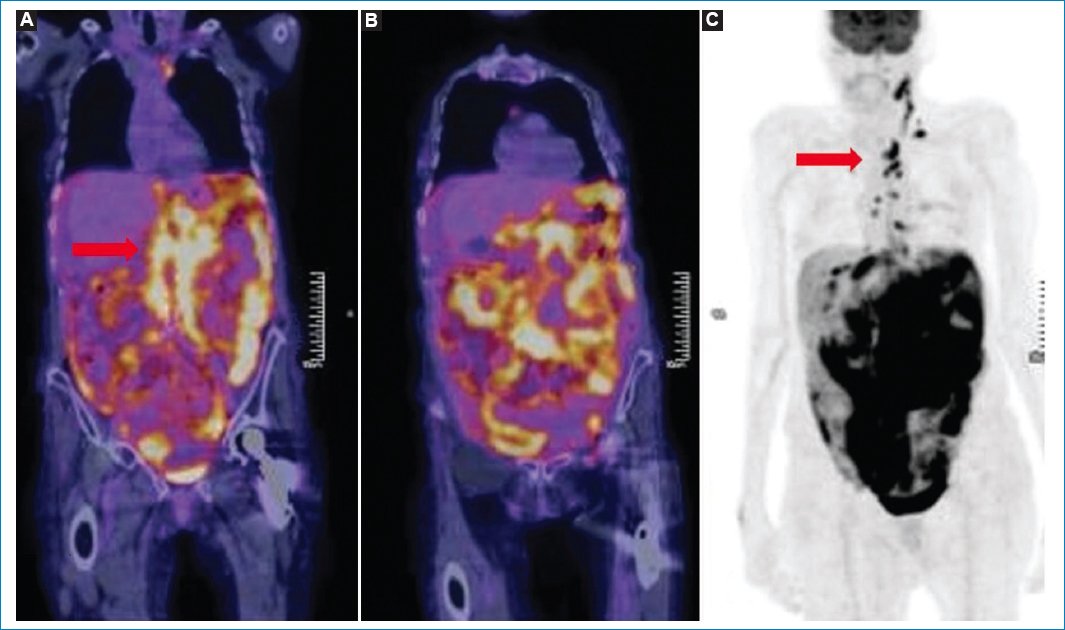
Figura 12. Imágenes coronales de fusión PET-TC (A y B) y MIP de PET (C) de un caso de LP. Como hallazgos acompañantes se evidencian múltiples adenomegalias hipermetabólicas en diferentes niveles ganglionares supra- e infradiafragmáticos (flechas).
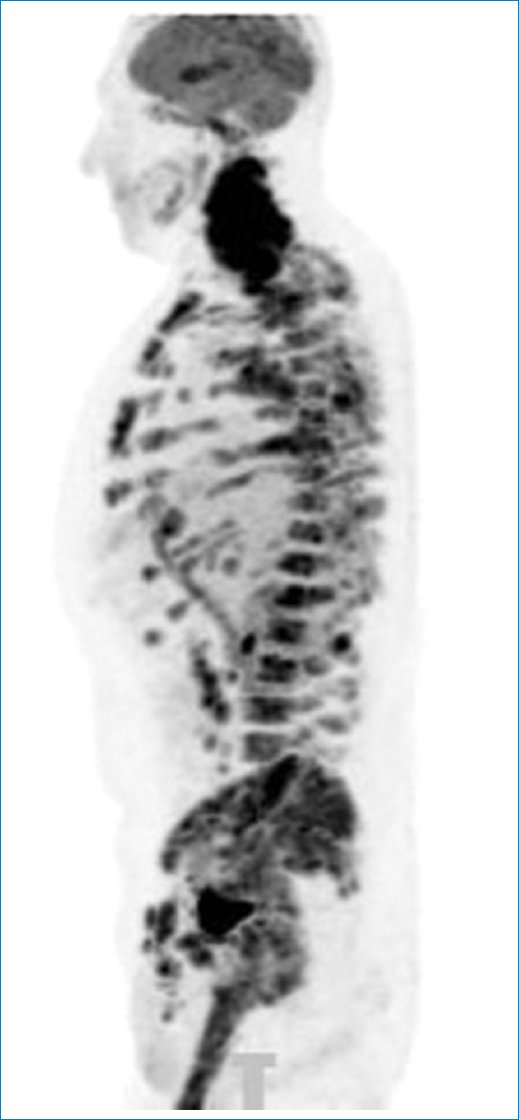
Figura 13. Imagen sagital en MIP de PET-TC que pone de manifiesto el hipermetabolismo de la médula ósea en un caso de linfoma con compromiso ganglionar múltiple y peritoneal.
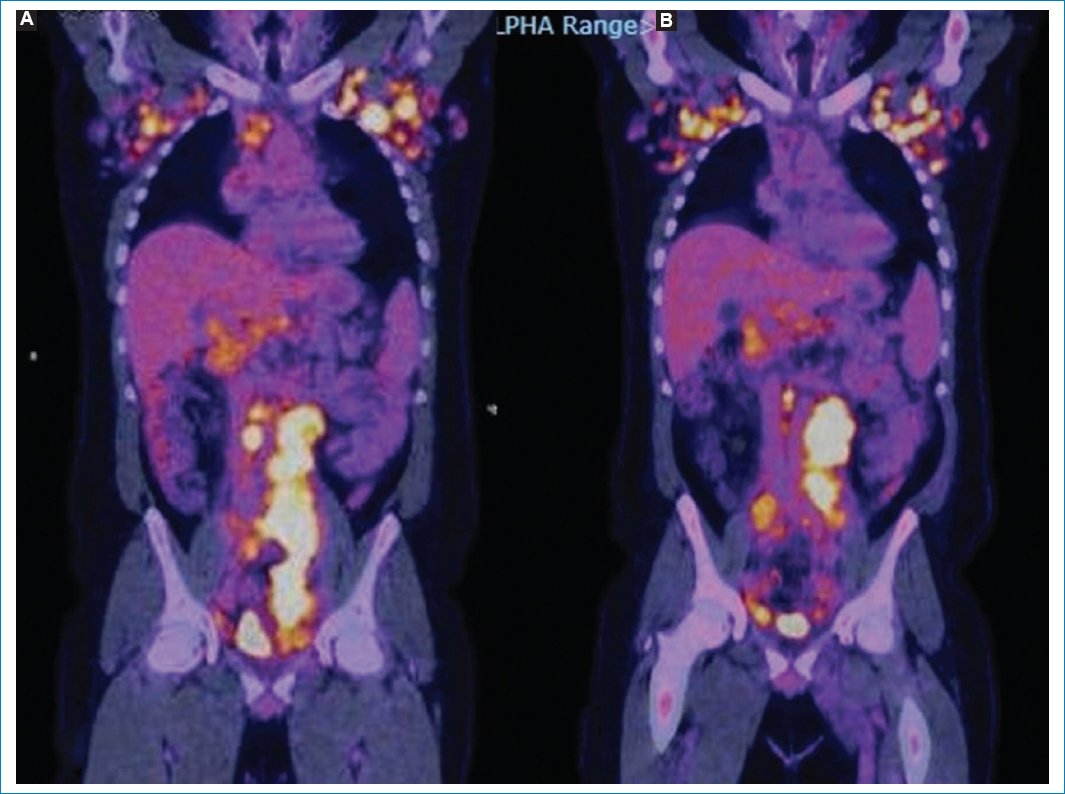
Figura 14. Paciente de 70 años con linfoma agresivo de alto grado, sin respuesta al tratamiento instaurado. Imagen coronal de fusión PET-TC pretratamiento (A) y postratamiento (B).
Según Cabral et al.11, el patrón más frecuente de presentación de la LP consiste en la observación del omental cake hipermetabólico, con conglomerados ganglionares múltiples (Fig. 15). El compromiso peritoneal aislado, sin afectación ganglionar, es extremadamente inusual33.
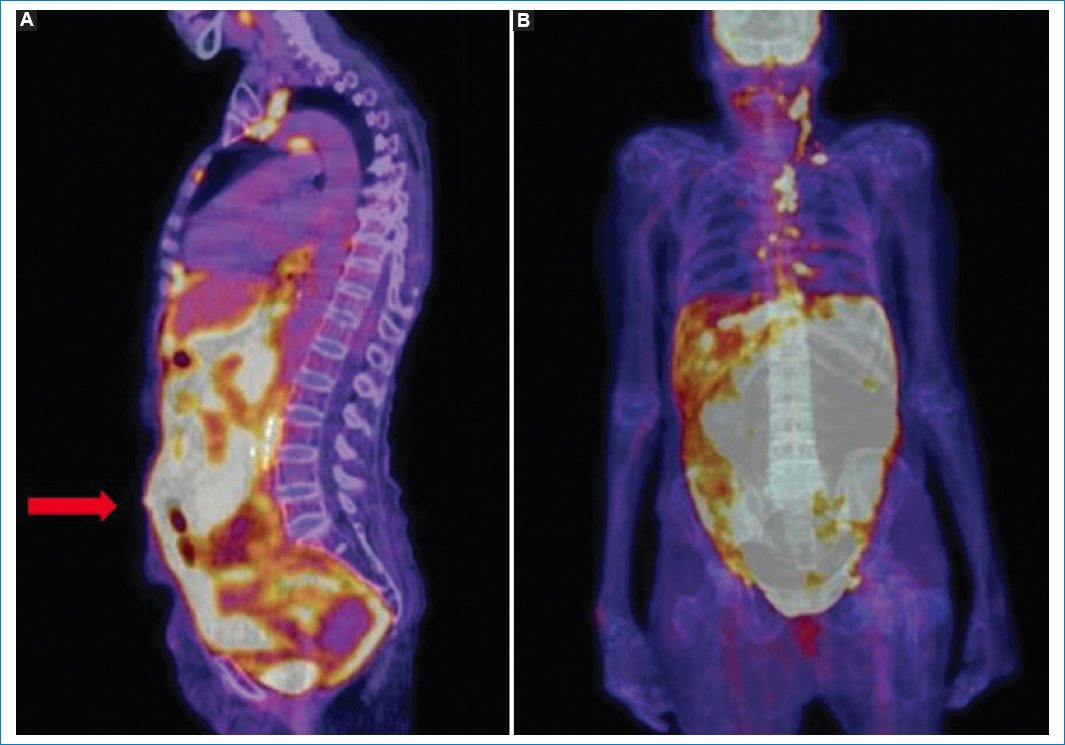
Figura 15. Patrón más frecuente de presentación de la LP, con compromiso difuso peritoneal hipermetabólico (omental cake, flecha) y adenomegalias múltiples; hallazgos evidentes en las imágenes de fusión PET-TC en sagital (A) y coronal (B).
Algunos autores, como Benameur et al.34 y Roy et al.35, han introducido un concepto nuevo respecto a la LP, el “superescáner peritoneal”, para referirse a los casos de hipermetabolismo difuso y excesivo de la 18F-FDG por el peritoneo, con el consiguiente menor consumo glucídico por el resto del cuerpo, en particular del cerebro, el corazón y los riñones (Fig. 16). Este concepto se denomina así por su similitud con el del “superescáner óseo” en el estudio centellográfico para el compromiso difuso del hueso34.
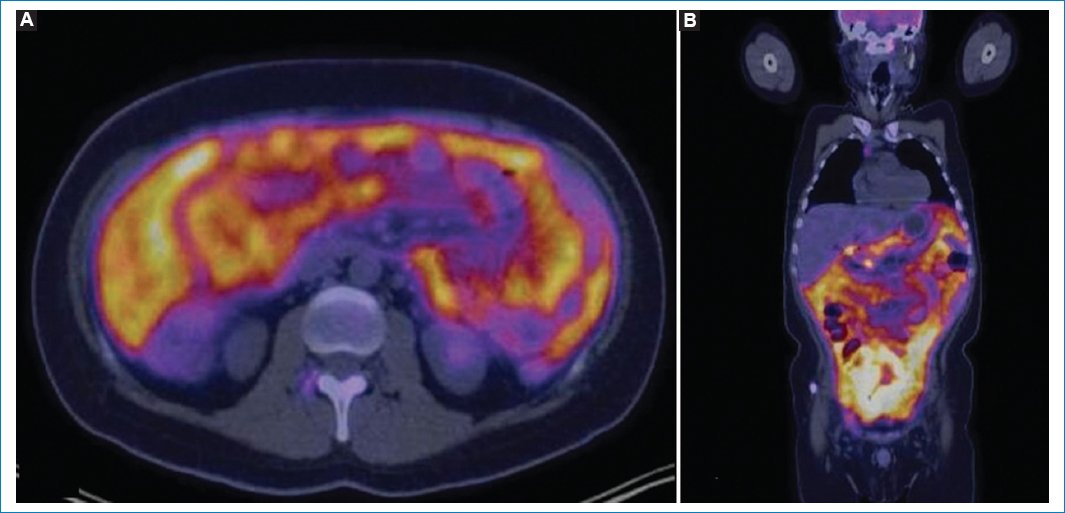
Figura 16. Imágenes axial (A) y coronal (B) de fusión PET-TC en un caso de “superescáner peritoneal”, con excesivo consumo de 18F-FDG por el peritoneo y el consecuente menor metabolismo del encéfalo, el corazón y los riñones.
Para el diagnóstico de la LP, la PET-TC tiene mayor sensibilidad que la TC, así como para observar sitios de afectación extranodal, incluso en ausencia de hallazgos tomográficos. Se estima una sensibilidad cercana al 100% y una especificidad superior al 97% para la detección de la siembra peritoneal, mientras que la TC tiene una sensibilidad del 88% y una especificidad del 97%11.
En general, la LP se acompaña de un deterioro progresivo en las condiciones del paciente, siendo de suma importancia su sospecha para iniciar un tratamiento óptimo y dirigido36. El compromiso peritoneal en el linfoma se considera de mal pronóstico para el paciente, y más aún si se acompaña de ascitis25. La LP puede conducir a un síndrome compartimental abdominal, con aumento de la presión intraabdominal, seguido por un compromiso en la perfusión renal, oliguria y fallo multiorgánico. Por estos motivos, la LP es una causa que eleva la morbimortalidad de estos pacientes34.
Su tratamiento consiste en quimioterapia similar a la utilizada para casos agresivos de linfoma, reportándose un 25% de respuesta y una consecuente mejoría en su pronóstico36 (Fig. 17). Sin tratamiento, la tasa media de supervivencia es menor de 1 año16,37.
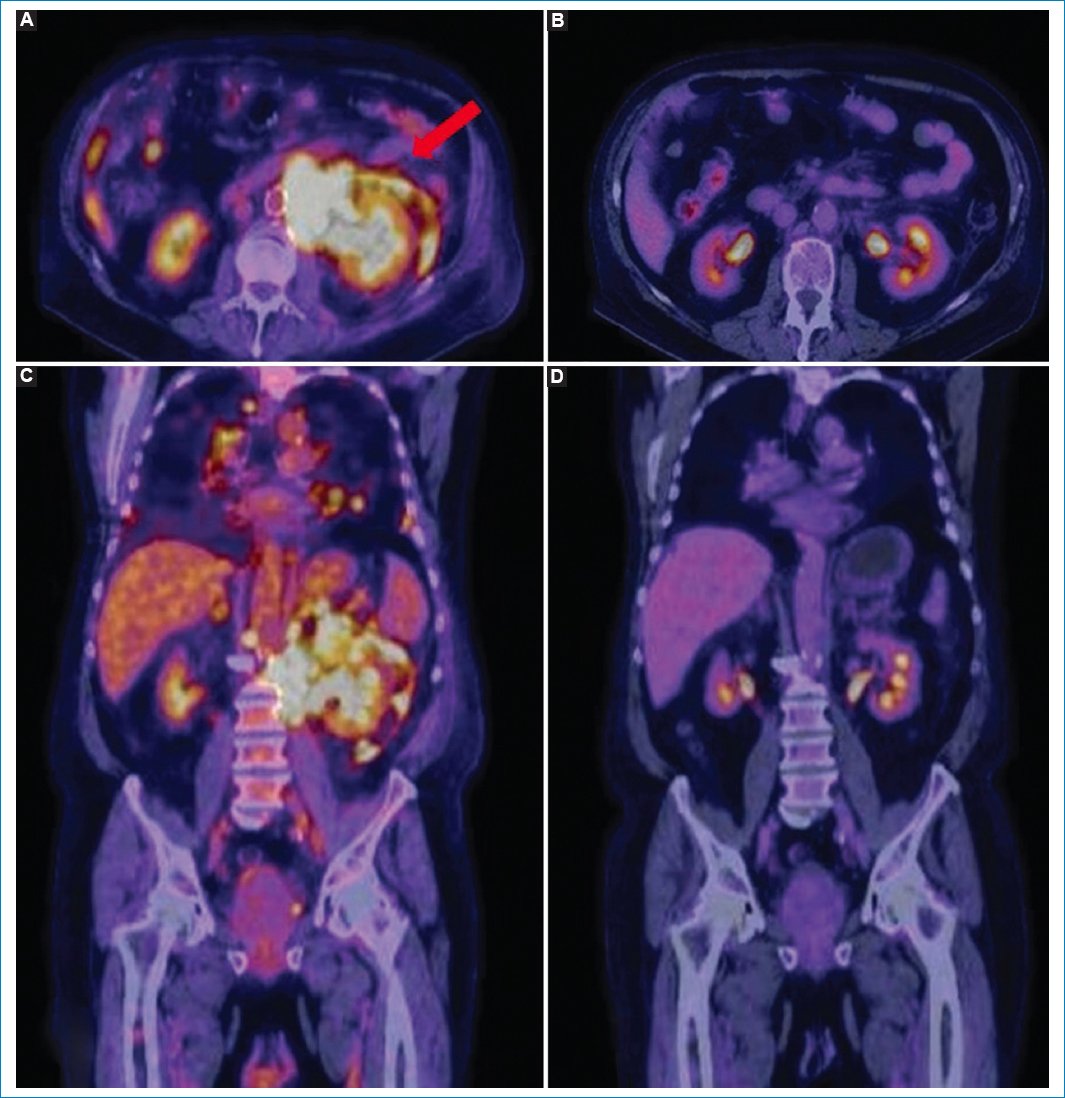
Figura 17. Paciente de 72 años con linfoma no Hodgkin testicular difuso de células B grandes, con LP al momento del diagnóstico (flecha en imagen en axial [A] y en coronal [C]), que luego del tratamiento recibido, con las imágenes comparativas más representativas, muestra buena respuesta (imágenes axial [B] y coronal [D]).
Debido al mal pronóstico que conlleva la afectación peritoneal como patología extranodal en el linfoma, resulta muy importante su conocimiento, tomando la PET-TC con 18F-FDG un rol protagónico para su diagnóstico. Este método se constituye como de elección para evaluar los linfomas, con características distintivas para el diagnóstico de la LP, permitiendo así arribar a un diagnóstico temprano y un oportuno tratamiento dirigido16.
Conclusión
Resulta fundamental el reconocimiento del compromiso peritoneal por el linfoma, denominado LP, para evitar diagnósticos erróneos por su similitud con la carcinomatosis peritoneal.
La PET-TC con 18F-FDG es el método de elección para su sospecha y diagnóstico. Deberá ser considerada en el paciente con diagnóstico de linfoma que presente formaciones nodulares hipermetabólicas en el peritoneo o hipermetabolismo difuso omental, asociado a adenomegalias y esplenomegalia.
Financiamiento
Los autores declaran no haber recibido financiamiento para este estudio.
Conflicto de intereses
Los autores declaran no tener conflicto de intereses.
Consideraciones éticas
Protección de personas y animales. Los autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad, consentimiento informado y aprobación ética. Los autores han seguido los protocolos de confidencialidad de su centro sanitario/institución para acceder a los datos de las historias clínicas. Se ha obtenido el consentimiento informado de los pacientes y se cuenta con la aprobación del Comité de Ética. Se han seguido las recomendaciones de las guías SAGER.
Declaración sobre el uso de inteligencia artificial. Los autores declaran que no se utilizó ningún tipo de inteligencia artificial generativa para la redacción ni la creación de contenido de este manuscrito.