Estimados Editores:
El objetivo de esta carta es mostrar las características imagenológicas de las patologías presentadas, que son infrecuentes pero con una alta tasa de mortalidad, para permitir su oportuno diagnóstico.
El síndrome de Lemierre es una enfermedad potencialmente mortal que afecta a adolescentes y adultos jóvenes. Se caracteriza por el antecedente reciente de una infección orofaríngea junto a tromboflebitis séptica de la vena yugular interna con diseminación embolígena a distintas partes del cuerpo. Su etiología es, en general, una infección por microorganismos anaerobios1.
Según las últimas revisiones, presenta mayor incidencia en el sexo masculino y se manifiesta con fiebre, odinofagia, cervicalgia y masa cervical. Fusobacterium necrophorum es el patógeno más frecuentemente aislado. Se ha descrito la presencia de émbolos en los pulmones, los huesos, las articulaciones y el sistema nervioso central2,3. El tratamiento se basa en antibioticoterapia y anticoagulación1–3.
Los pseudoaneurismas de las arterias pulmonares son consecuencia de un daño en la pared vascular, y al no estar contenidos por las capas normales son inestables y pueden romperse con el consecuente sangrado hacia el parénquima pulmonar o la luz bronquial. Suelen originarse en las arterias pulmonares, aunque también pueden afectar a las arterias bronquiales. Clínicamente se manifiestan con tos y hemoptisis4.
Pueden tener múltiples etiologías, siendo la infecciosa la más frecuente, por extensión directa de una neumonía adyacente (el ejemplo clásico es el pseudoaneurisma de Rasmussen secundario a una infección tuberculosa). También se han descrito en pacientes con enfermedad pulmonar émbolo-séptica y otras etiologías, como son la enfermedad neoplásica primaria o metastásica, lesiones traumáticas, tromboembolia pulmonar, hipertensión pulmonar o vasculitis. El tratamiento es endovascular, con coils o stents4,5.
Presentamos el caso de una paciente de 12 años que consulta por fiebre, tumoración dolorosa en la región anterior del cuello y tos con expectoración. Como antecedente, presentó odinofagia y fiebre 15 días antes, que se interpretó como faringoamigdalitis, sin clara mejoría posterior al tratamiento antibiótico dirigido.
En la exploración física se constató palidez cutánea y mucosa, con mal estado general, taquicardia, taquipnea, hipotensión, temperatura de 39 °C, faringe congestiva e hipoventilación en ambos campos pulmonares inferiores. Las pruebas de laboratorio evidenciaron anemia, leucocitosis, plaquetopenia, aumento de los reactantes de fase aguda, tiempo de protrombina prolongado e hiponatremia.
Se solicitó radiografía de tórax, que evidenció acentuación de la trama peribroncovascular de predominio pulmonar derecho e infiltrado intersticial bibasal sin consolidación evidente. Se realizó ecografía del cuello, en la que se visualizó una colección hipoecoica en situación anterior a la glándula tiroides y trombosis de la vena yugular derecha.
Se internó en la unidad de terapia intensiva por sospecha clínica de shock séptico secundario a un absceso perifaríngeo complicado con mediastinitis. Se complementó la evaluación con tomografía computada multislice (TCMS) de cuello (Fig. 1) y tórax con contraste (Fig. 2) para evaluar la extensión de la colección a los espacios retrofaríngeos y al mediastino anterior.
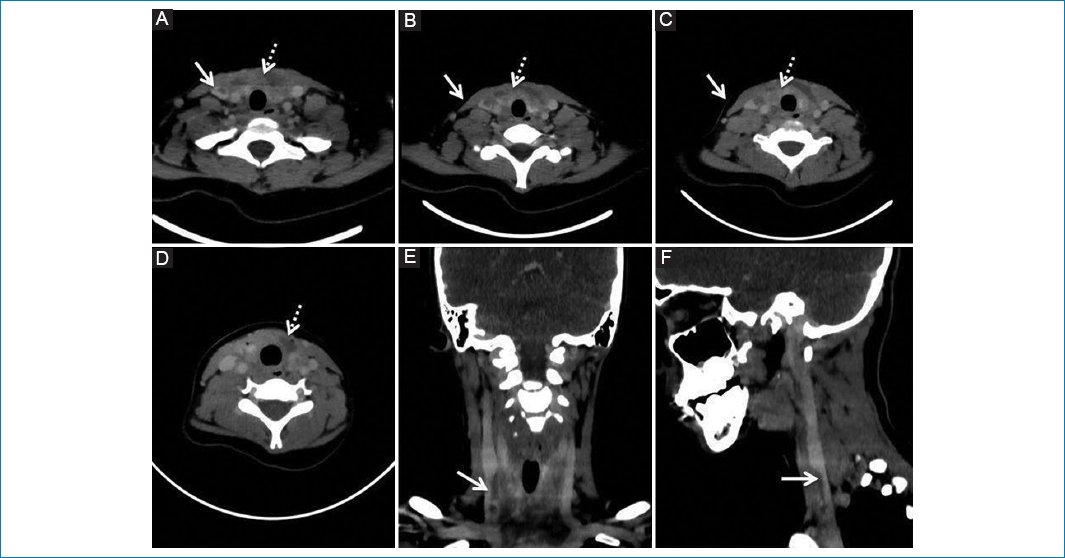
Figura 1. TCMS de cuello con contraste, cortes axiales (A, B, C, D), coronal (E) y sagital (F). En proyección anterior a la glándula tiroides, y comprometiendo al espacio carotídeo derecho, se visualiza una colección de contenido hipodenso, presencia de burbujas y refuerzo de la pared tras la inyección de la sustancia de contraste (flecha punteada), así como trombosis del tercio distal de la vena yugular interna derecha en proximidad al confluente yúgulosubclavio (flecha).
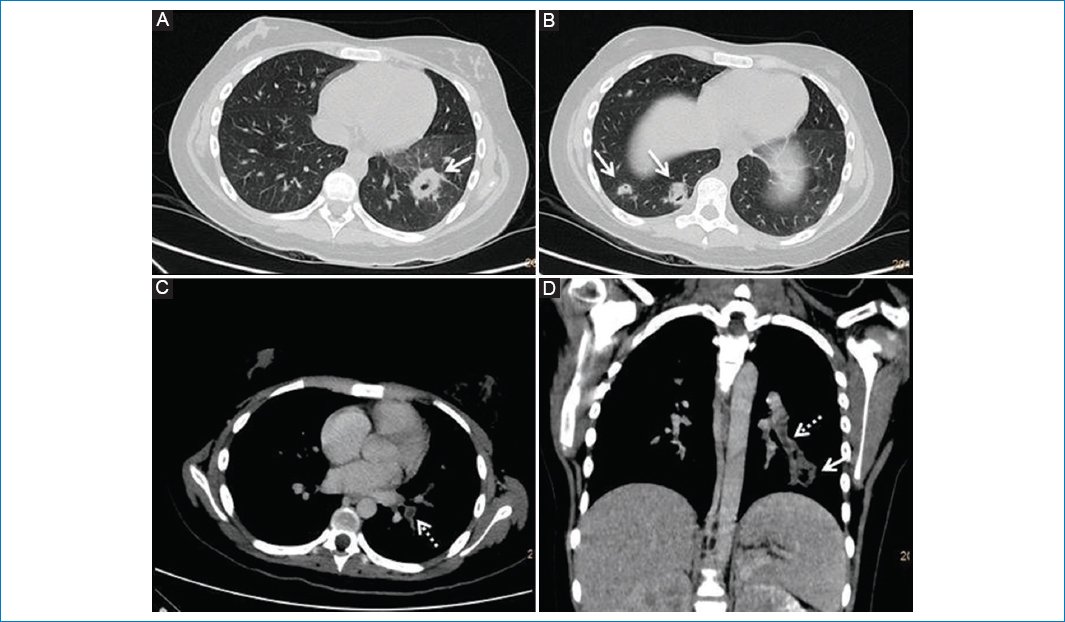
Figura 2. TCMS de tórax con contraste, cortes axiales (A, B, C) y coronal (D). Se visualizan múltiples formaciones nodulares, de tamaño variable, en ambos campos pulmonares (flecha), dos de ellas cavitadas, localizadas en el segmento posterior del lóbulo inferior derecho y en el segmento posterior del lóbulo inferior izquierdo (flecha). Todas presentan realce tras la inyección de contraste y se interpretan como abscesos. En los vasos pulmonares de los segmentos inferiores izquierdos se observa hipodensidad en relación con un defecto de relleno, que se interpreta como tromboembolia pulmonar (flecha punteada).
A las dos semanas de ingreso, tras un episodio de hemoptisis se realizó angio-TCMS de tórax, en la cual se observó la cavitación ya conocida ocupada por contenido de densidad similar a los vasos pulmonares, sugestivo de extravasación del material de contraste, rodeada de opacidad difusa en vidrio esmerilado en relación con hemorragia pulmonar. Además, se visualizaron trombosis de la arteria segmentaria ánteromedial del lóbulo inferior izquierdo y al menos tres dilataciones fusiformes y sucesivas en la arteria del segmento posterior del lóbulo inferior izquierdo, en relación con dilataciones pseudoaneurismáticas (Fig. 3).
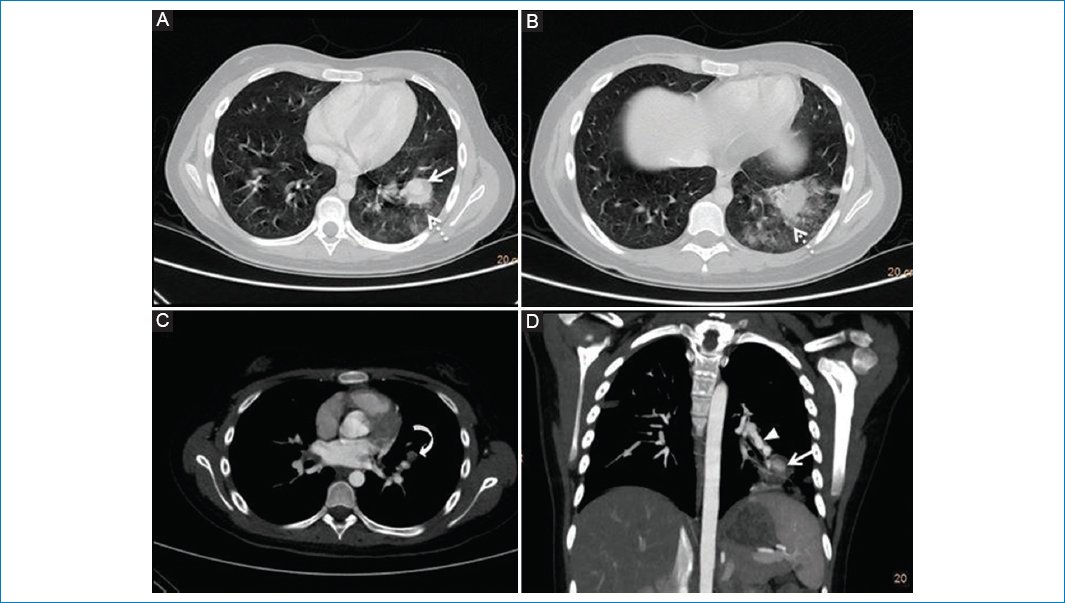
Figura 3. Angio-TCMS de tórax, cortes axiales (A, B, C) y coronal (D). En el segmento posterior del lóbulo inferior derecho se observa una cavitación ocupada por contenido de densidad similar a los vasos pulmonares, sugestivo de extravasación del material de contraste (flecha), rodeada de opacidad difusa en vidrio esmerilado en relación con hemorragia pulmonar (flecha punteada). Además, se visualizan trombosis de la arteria segmentaria ánteromedial del lóbulo inferior izquierdo (flecha curva) y al menos tres dilataciones fusiformes y sucesivas en la arteria del segmento posterior del lóbulo inferior izquierdo, dándole a la misma un aspecto arrosariado en relación con dilataciones pseudoaneurismáticas (punta de flecha).
Posteriormente, se realizó arteriografía de los vasos pulmonares para su tratamiento endovascular (Fig. 4).
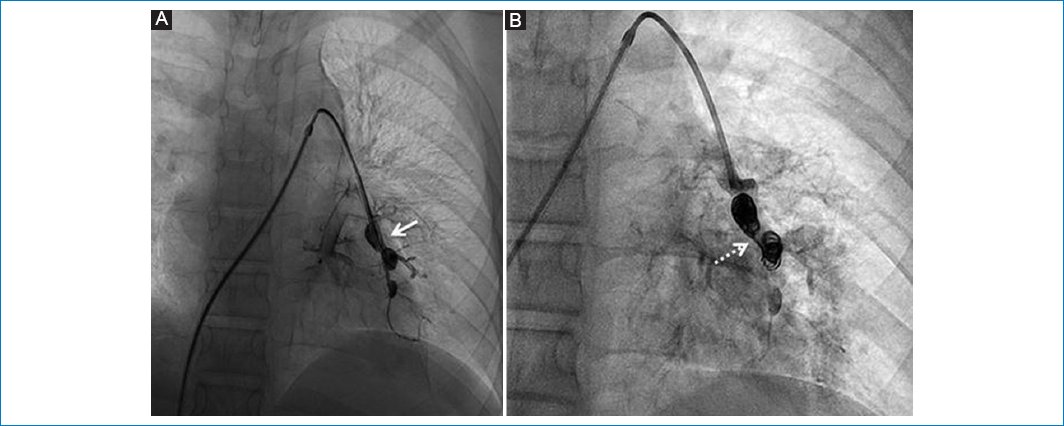
Figura 4. Arteriografía pulmonar. (A) Identificación de sacos pseudoaneurismáticos (flecha). (B) Embolización (flecha punteada).
Durante la internación se realizaron hemocultivos, que resultaron negativos, y punción percutánea bajo guía ecográfica de la colección cervical, donde se rescató Staphylococcus epidermidis, que se interpretó como muestra contaminada.
La paciente evolucionó favorablemente y tras completar el tratamiento se externó un mes después de su ingreso.
Financiamiento
Los autores declaran no haber recibido financiamiento para este estudio.
Conflicto de intereses
Los autores declaran no tener conflicto de intereses.
Consideraciones éticas
Protección de personas y animales. Los autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad, consentimiento informado y aprobación ética. Los autores han seguido los protocolos de confidencialidad de su institución, han obtenido el consentimiento informado de los pacientes, y cuentan con la aprobación del Comité de Ética. Se han seguido las recomendaciones de las guías SAGER, según la naturaleza del estudio.
Declaración sobre el uso de inteligencia artificial. Los autores declaran que no han utilizado ningún tipo de inteligencia artificial generativa en la redacción de este manuscrito.