Estimados editores:
El carcinoma fibrolamelar (CFL) es una variante infrecuente del carcinoma hepatocelular (HCC), con una presentación clínica inespecífica en etapas iniciales. Afecta a ambos sexos, predomina en adultos jóvenes, menores de 40 años y sin antecedentes de enfermedad hepática1,2.
Se considera una neoplasia agresiva con una supervivencia a cinco años de menos del 50%, siendo el factor principal determinante de mal pronóstico una enfermedad estadio IV al momento del diagnóstico1,3.
Si bien la tríada clásica de esta entidad es la de dolor abdominal, masa palpable en hipocondrio derecho y pérdida de peso, algunos, como en el caso de nuestra paciente, pueden ser indolentes4.
Presentamos el caso de una mujer de 29 años de edad, previamente sana, sin antecedentes relevantes. Consultó por un cuadro clínico de amenorrea y dolor lumbar de tres meses de evolución, por lo que se realiza ecografía abdominal que informa una lesión tumoral sólida en el lóbulo hepático derecho. El día de la consulta presentó un episodio aislado de convulsión tónico-clónica generalizada, por lo que se decide internación. La tomografía computada (TC) de cerebro confirmó la presencia de lesión ocupante de espacio a nivel frontoparietal izquierdo, de aparente origen extraaxial con extensa base dural, extensión a la calota y marcado realce tras la administración del contraste endovenoso (Fig. 1). En relación con el parénquima hepático, se observó en TC de abdomen imagen heterogénea que ocupaba casi en la totalidad el lóbulo hepático derecho, asociada a lesiones satélites bilaterales, sin signos de daño hepático crónico (Fig. 2). Por último, como datos positivos se constató la presencia de un trombo en la vena porta (Fig. 3) e imágenes de aspecto secundario en estructuras óseas vertebrales y en calota. La resonancia magnética (RM) de cerebro con gadolinio evidenció compromiso intraaxial y extraaxial de la lesión cerebral (Fig. 4).
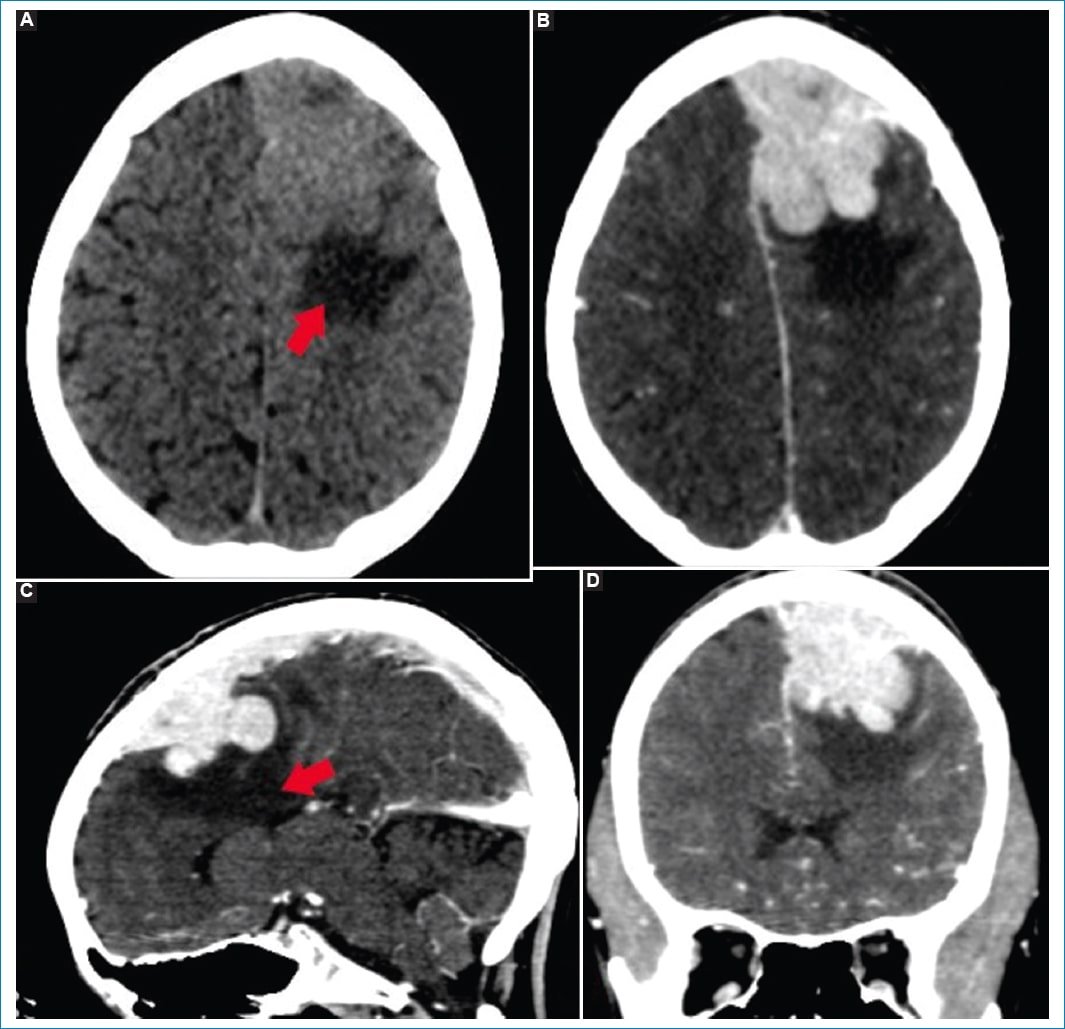
Figura 1. TC de cerebro. A: plano axial, presenta imagen hiperdensa, lobulada, en lóbulo frontal izquierdo con signos de edema perilesional (flecha roja). B, C y D: planos axial, sagital y coronal respectivamente. Se muestra una lesión ocupante de espacio, que impresiona de origen extraaxial y genera desplazamiento de la línea media, con marcado realce tras la administración del contraste iodado endovenoso.
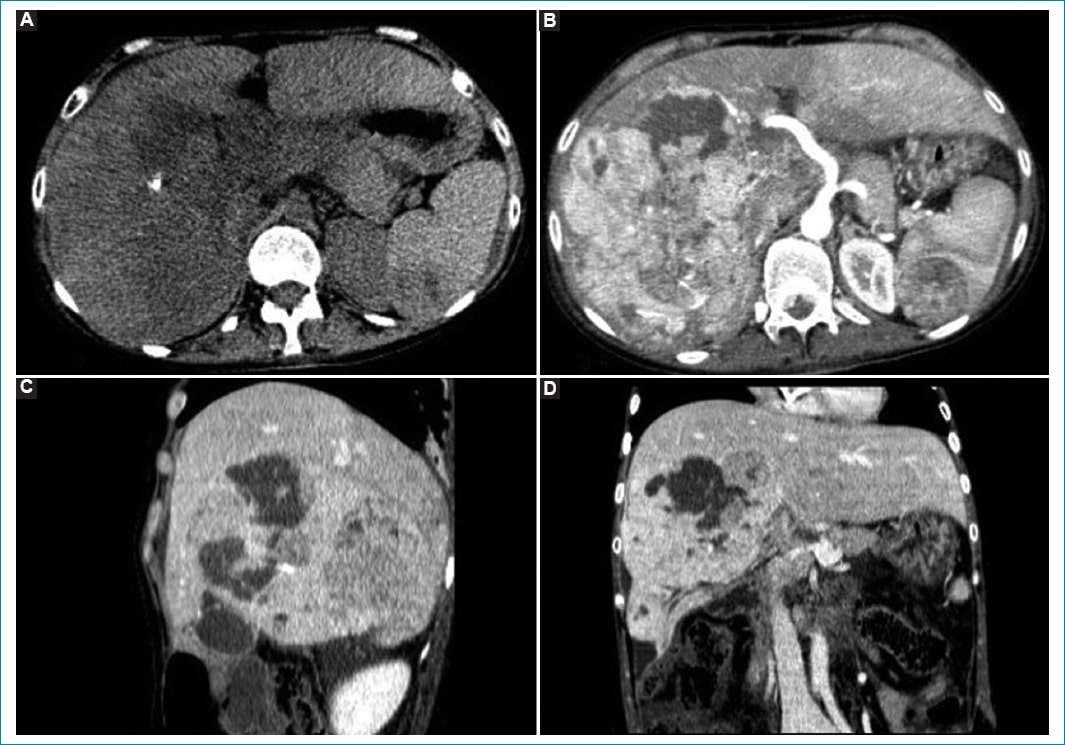
Figura 2. TC de abdomen y pelvis. A: se visualiza parénquima hepático heterogéneo en forma difusa con áreas de densidad líquida y cálcica. B: en tiempo arterial se observa imagen heterogénea con marcado realce que compromete predominantemente el lóbulo derecho hepático. Presenta área central hipodensa y áreas cálcicas periféricas. C y D: planos sagital y coronal en tiempos venosos que evidencian la formación hepática marcadamente heterogénea.
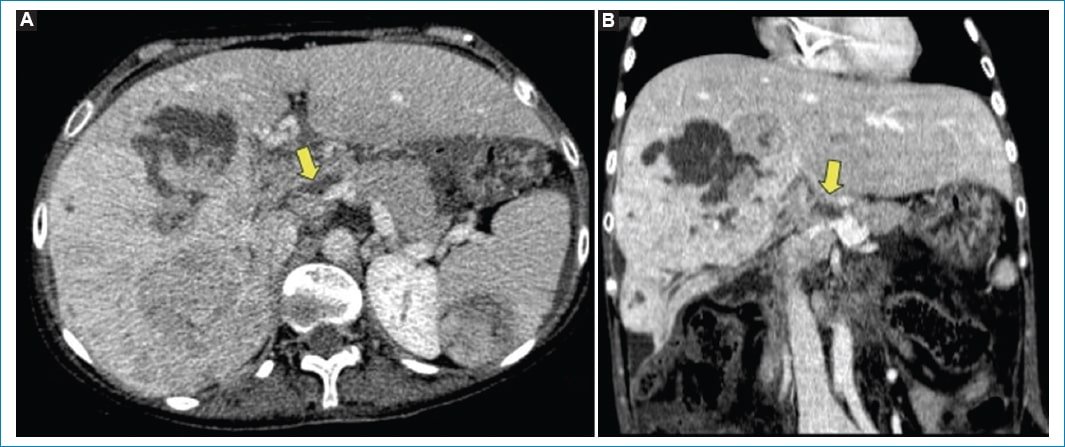
Figura 3. TC de abdomen y pelvis en tiempo venoso. A: plano axial. B: plano coronal. Se visualiza en vena porta defecto de relleno hipodenso (flecha amarilla), en relación con trombo portal.
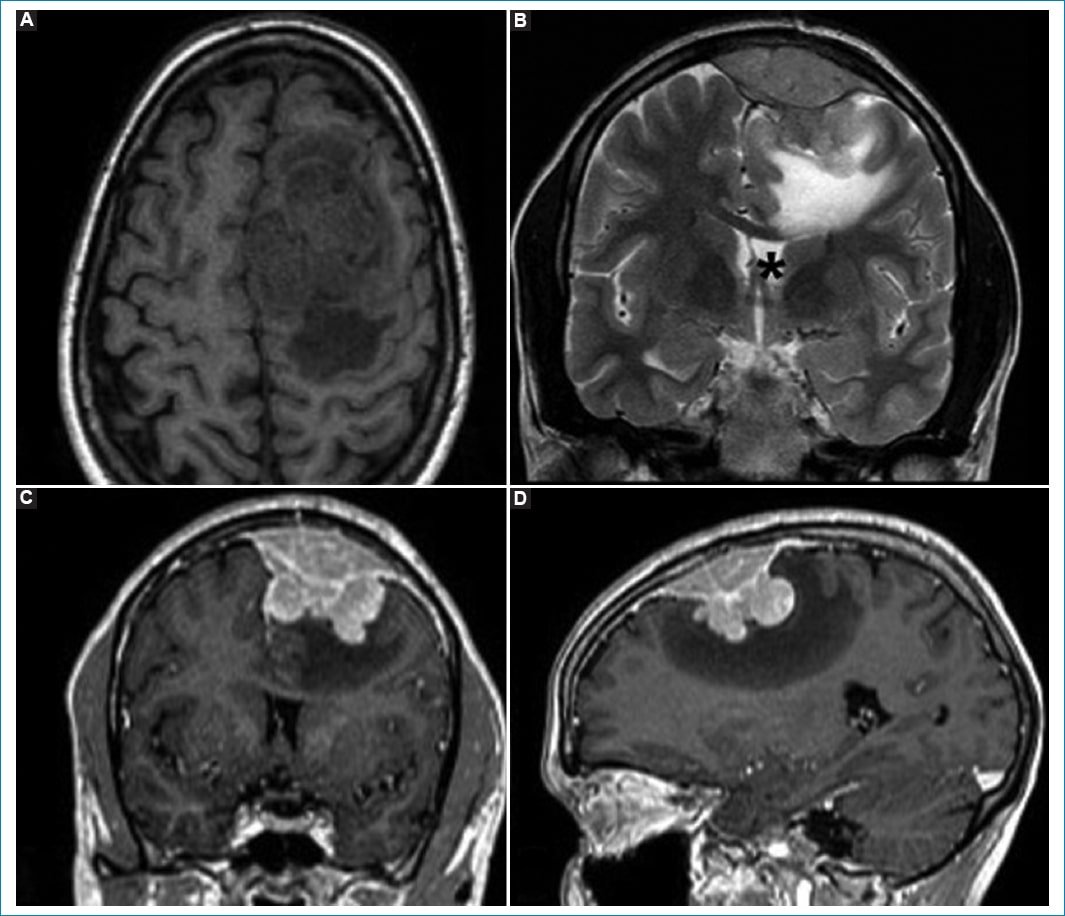
Figura 4. RM de cerebro. A: secuencia potenciada en T1 sin gadolinio. Se visualiza a nivel frontal izquierdo imagen heterogénea, lobulada, que genera desviación de la línea media. B: secuencia potenciada en T2, plano coronal. Se observa compromiso extraaxial con edema perilesional y colapso ventricular homolateral (*). C y D: T1 con gadolinio, planos sagital y coronal. Evidencia lesión lobulada intraaxial y extraaxial con refuerzo dural y marcado realce de esta tras la administración del contraste, edema adyacente, desviación de línea media y efecto de masa sobre ventrículo lateral.
El estudio de los virus hepatitis B y C fue negativo y los niveles de alfafetoproteína y CA 19-9 fueron normales. Se realizó una biopsia de la lesión de origen extraaxial con extensión y compromiso de calota, cuyos hallazgos morfológicos e inmunohistoquímicos fueron compatibles con HCC, variante fibrolamelar.
Estos tumores se presentan más comúnmente como masas bien delimitadas caracterizadas microscópicamente por células poligonales grandes con abundante citoplasma eosinófilo y nucléolo grande. El término fibrolamelar se utiliza por la presencia de bandas fibrosas de colágeno que rodean estas células4.
En el CFL los marcadores de la función hepática son normales o pueden estar levemente elevados, a diferencia de lo que sucede en el HCC, donde la alfafetoproteína usualmente se encuentra elevada5. Algunos de los factores pronósticos de malignidad son hallazgos tales como tumores múltiples, invasión vascular y ganglios linfáticos positivos1,6.
El diagnóstico se realiza mediante la base de la presentación clínica en conjunto con los hallazgos imagenológicos, aunque para casos indeterminados se puede utilizar la biopsia con aguja gruesa guiada por TC o la aspiración con aguja fina5.
En la ecografía, el CFL se caracteriza como una masa bien definida con ecogenicidad heterogénea. En la TC con contraste endovenoso suele presentarse como una masa grande, heterogénea, de contorno lobulado y en RM suelen ser hipointensos en las imágenes ponderadas en T1 e hiperintensos en T2 con una cicatriz central fibrosa hipointensa en todas las secuencias1,5. Esta es clave para poder realizar diagnóstico diferencial con masas hepáticas benignas, como la hiperplasia nodular focal (HNF), que típicamente tiene una cicatriz central predominantemente hiperintensa en las secuencias potenciadas en T2. Las características en RM que pueden determinar el diagnóstico imagenológico de CFL sobre la HNF son una mayor heterogeneidad del componente de la lesión, incluidas la necrosis y la hemorragia, la hipointensidad de la cicatriz central del CFL potenciadas en T2, aunque puede ser variable y el hiporrealce de la vena portal7. En la RM con gadolinio, el CFL se caracteriza por un marcado realce heterogéneo en fase arterial que homogeniza en fase venosa portal.
Es necesario diferenciarlo de otros tumores hipervasculares como el adenoma hepático o el HCC convencional. El adenoma, en contraste con el CFL, muestra un realce homogéneo en fase arterial. El CFL puede tener áreas con densidad grasa, en contraste con el HCC convencional6.
Existen en la literatura pocos casos reportados de metástasis cerebrales del CFL. Sus presentaciones fueron sólido-quísticas, con desviación de la línea media y marcado realce poscontraste8.
El tratamiento inicial de elección para el CFL, siempre que sea posible, es la resección quirúrgica agresiva junto con linfadenectomía regional para la enfermedad primaria9. Es de gran importancia considerar la resección repetida o el trasplante hepático ortotópico para estos tumores, dada la falta de terapias alternativas eficaces1,8. Se sugiere realizar seguimiento de los pacientes durante al menos diez años, dada la alta tasa de recidiva2.
En la revisión de la bibliografía de otros tres casos reportados8 no es clara la evolución del curso clínico de la enfermedad desde su inicio al desarrollo de metástasis cerebrales. El diagnóstico de este tumor generalmente se realiza en etapas avanzadas, dada la ausencia de sintomatología en estadios iniciales, es por esto que resulta relevante ampliar el estudio con neuroimágenes ante el diagnóstico de CFL.
Financiamiento
Los autores declaran no haber recibido financiamiento para este estudio.
Conflicto de intereses
Los autores declaran no tener conflicto de intereses.
Responsabilidades éticas
Protección de personas y animales. Los autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datos. Los autores declaran que en este artículo no aparecen datos de pacientes.
Derecho a la privacidad y consentimiento informado. Los autores declaran que en este artículo no aparecen datos de pacientes.
Uso de inteligencia artificial para generar textos. Los autores declaran que no han utilizado ningún tipo de inteligencia artificial generativa en la redacción de este manuscrito ni para la creación de figuras, gráficos, tablas o sus correspondientes pies o leyendas.