Historia clínica
Paciente afroamericana/negra de 62 años con antecedentes médicos de hipertensión, diabetes mellitus no dependiente de insulina, enfermedad por reflujo gastroesofágico, enfermedad vascular periférica y también estado de cáncer de mama después de una mastectomía radical derecha que resultó en linfedema de la extremidad superior derecha. Inicialmente se presentó por dolor de cuello, y una resonancia magnética (RM) mostró una masa espinal. Un mes después se presentó al servicio de urgencias con quejas de debilidad generalizada, y entumecimiento de ambas extremidades inferiores e incapacidad para caminar. El tumor se sometió a una laminectomía C4-C7 con biopsia, después de lo cual hubo una ligera mejoría temporal de su debilidad del lado derecho. La paciente sobrevivió durante un mes después de la biopsia y durante dos meses desde el descubrimiento inicial de la masa en la RM.
Examen
Tos durante la ingestión de alimentos. Sensación de comida que no progresa después de tragar.
La disfagia mecánica es aquella en la que hay un obstáculo físico al paso del bolo, como ocurre, por ejemplo, en los tumores de células escamosas de cabeza y cuello.
La disfagia motora es aquella causada por la alteración o incoordinación de la deglución; aparece principalmente en enfermedades neurodegenerativas o musculares, o en situaciones que compliquen el inicio de la deglución (lesiones bucales, xerostomía, afectación de los nervios vago y/o glosofaríngeo, etc.). Un tumor en la médula cervical sí puede causar disfagia, especialmente si compromete C1-C4, por afectación bulbar, corticobulbar o mecánica secundaria, y debe considerarse una bandera roja neurológica1,2.
Resonancia magnética
Se aprecia un tumor intradural intramedular que tiene una extensión de cuatro vértebras, desde C3 a C6 (Figs. 1–4).
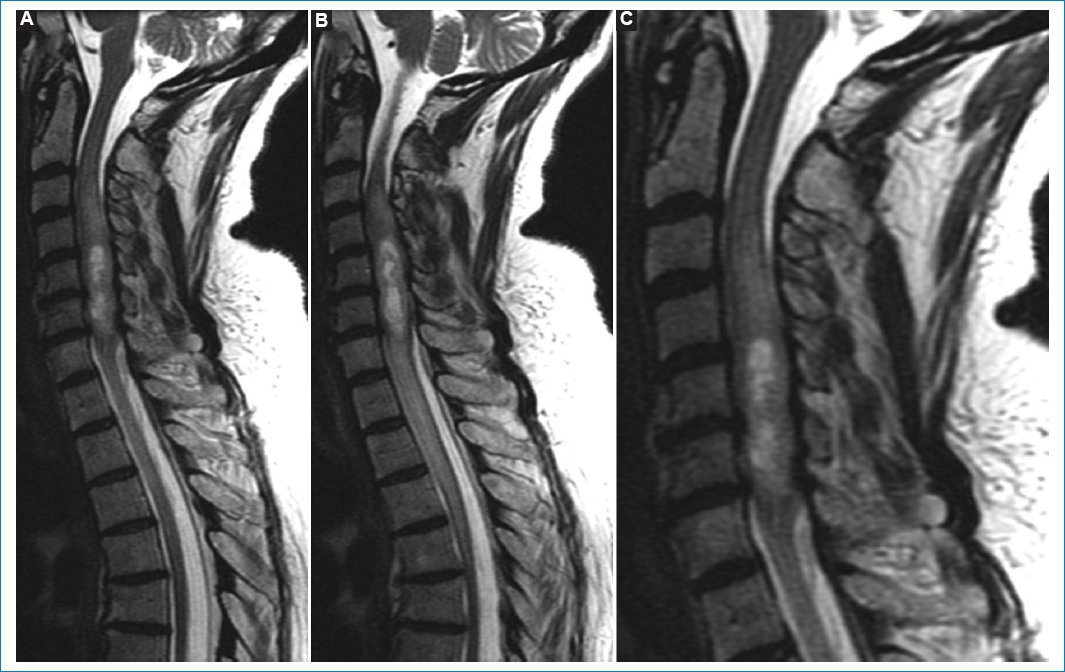
Figura 1. RM sagital ponderada en T2. Muestra aumento del tamaño de la médula espinal con centro de hiperintensidad intramedular difusa de extensión longitudinal, compatible con infiltración tumoral con centro quístico: cortes contiguos (A y B) y ampliación de A (C).
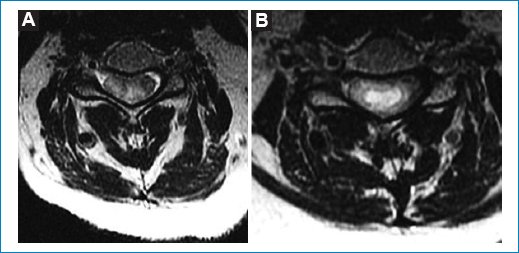
Figura 2. Secuencia axial ponderada en T2. Masa heterogénea. (A) Polo superior. (B) Centro donde predomina el componente quístico.
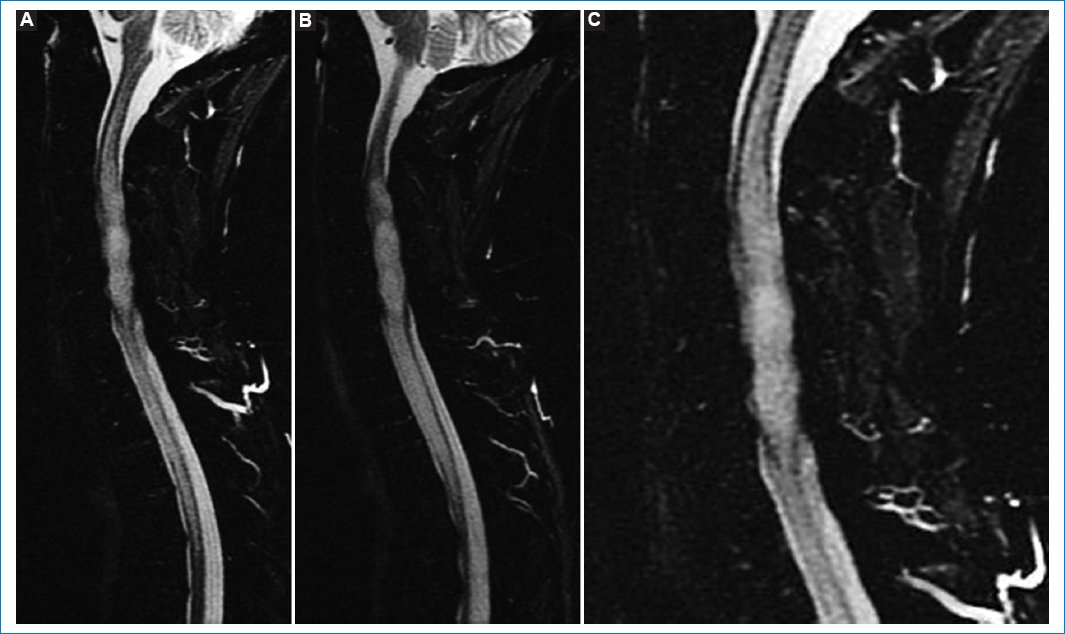
Figura 3. Secuencia STIR. (A) Corte central. (B) Corte contiguo. (C) Ampliación de A. Hiperintensidad extensa y homogénea de la médula espinal afectada que excede el volumen tumoral sólido que se verá en la secuencia ponderada en T1.
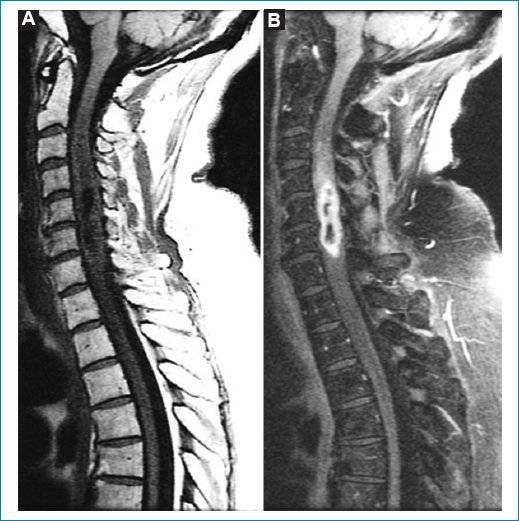
Figura 4. (A) Secuencia sagital ponderada para T1 sin contraste. (B) Secuencia sagital STIR después de administrar contraste paframagnético. Tras la administración de gadolinio en secuencia STIR se observa realce periférico en anillo (rim enhancement).
Tiene una posición central con una porción quística intratumoral. La lesión es isointensa en T1 e hiperintensa en T2 y STIR (Figs. 1–5). Después de administrar contraste paramagnético endovenoso hay realce periférico, especialmente alrededor de la formación quística. Por debajo del polo inferior se ve siringohidromielia de corto trayecto. Las características de las imágenes coinciden con las descripciones que aparecen en la bibliografía3–5.
Se realizó un análisis de textura6–9 (Tabla 1, Fig. 6) donde la varianza fue la métrica de textura que mostró la mayor desviación respecto al tejido normal en todas las secuencias analizadas, seguida por la media de intensidad y la curtosis, especialmente en T2 y STIR. La varianza, como métrica con mayor desviación respecto al tejido normal, sugiere una marcada heterogeneidad de la señal, consistente con infiltración tumoral, desorganización microestructural y la presencia de componentes necróticos y/o edematosos, particularmente evidentes en la secuencia STIR.
Tabla 1. Evaluación de la textura tisular
| Secuencia | Métrica | Desviación media absoluta |
|---|---|---|
| T1 | Varianza | 224,5 |
| Media | 40 | |
| Curtosis | 0,97 | |
| Asimetría | 0,44 | |
| T2 | Varianza | 121 |
| Media | 74,5 | |
| Curtosis | 69 | |
| Asimetría | 1,28 | |
| STIR | Varianza | 106,5 |
| Media | 27,5 | |
| Curtosis | 8,68 | |
| Asimetría | 1,85 | |
* Desviación media absoluta calculada como el promedio de las diferencias absolutas entre las regiones tumorales (superior y media) y el tejido normal.
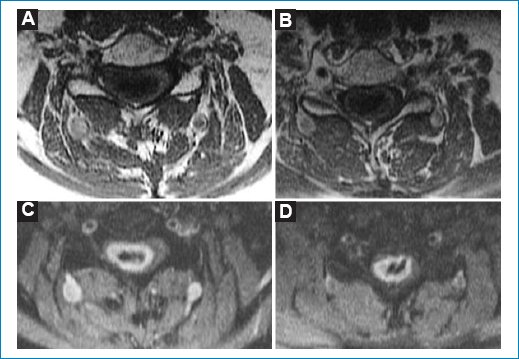
Figura 5. (A y B) Secuencia axial en dos niveles ponderada para T1. (B y C) Secuencia axial STIR en dos niveles después de administrar contraste endovenoso. Tras la administración de gadolinio, en secuencia STIR se observa realce periférico en anillo, compatible con heterogeneidad tumoral.
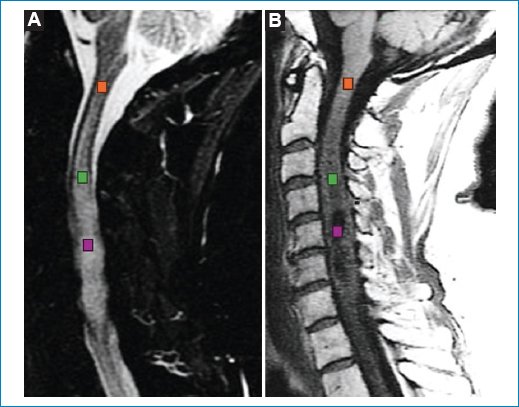
Figura 6. (A) Regiones de interés sobre una secuencia sagital ponderada para T2. (B) Regiones de interés sobre una secuencia sagital STIR. Naranja: normal. Verde: polo superior del tumor. Violeta: centro del tumor.
La varianza fue la métrica de textura que mostró la mayor desviación respecto al tejido normal en todas las secuencias analizadas, seguida por la media de intensidad y la curtosis, especialmente en T2 y STIR.
Imágenes de patología
El estudio histopatológico revela una neoplasia glial difusa, altamente celular, integrada por células tumorales con núcleos hipercromáticos y pleomorfismo moderados, con actividad mitótica aumentada. La inmunohistoquímica (IHQ) demuestra expresión difusa de proteína ácida fibrilar glial (GFAP), confirmando el origen glial.
Se observa positividad nuclear intensa y extensa para histona H3 K27M, hallazgo diagnóstico de glioma difuso de la línea media, H3 K27-alterado. El índice de proliferación evaluado mediante Ki-67 es elevado, en concordancia con un tumor de alto grado.
H3 K27M se refiere a una mutación genética específica (lisina a metionina en la posición 27) en la proteína histona H3, un sello distintivo de los tumores cerebrales agresivos pediátricos y adultos llamados “gliomas difusos de la línea media”, a menudo ubicados en el tronco encefálico, el tálamo y la médula espinal, conocidos por malos resultados a pesar de la radiación estándar, lo que lleva a una intensa investigación para terapias dirigidas como vacunas y nuevos medicamentos.
La proteína histona H3 es una proteína que se envuelve alrededor del ADN, actuando como un interruptor para la actividad genética.
La mutación K27M consiste en un cambio de lisina (K) a metionina (M) en la posición 27 de la proteína H3. Esta mutación altera la regulación genética normal, haciendo que las células se comporten como células madre cerebrales inmaduras, lo que lleva a un crecimiento descontrolado.
De acuerdo con la clasificación vigente de la Organización Mundial de la Salud (OMS), la identificación de la alteración H3 K27 define per se un tumor grado IV, independientemente de los criterios histológicos clásicos. Este subtipo se asocia a un curso clínico agresivo y mal pronóstico, subrayando la importancia de la integración morfológica, IHQ y molecular para un diagnóstico preciso.
Análisis histológico
Las secciones de la muestra de biopsia, fijadas con formalina e incluidas en parafina, se tiñeron con hematoxilina-eosina (H&E) y se procesaron para IHQ con GFAP (EP672Y), p53 (DO-7), Ki-67 (30-9) (Roche/Ventana Medical Systems Inc., Tucson, AZ, EE.UU.) e histona H3-K27M (Millipore/Sigma, Burlington, MA, EE.UU.), como se describió previamente10.
La biopsia mostró una neoplasia infiltrante hipercelular compuesta por pequeñas células “azules” con núcleos redondos hipercromáticos y escaso citoplasma o, de forma más focal, por células fibrilares con núcleos hipercromáticos alargados (Fig. 7). El tumor mostró una actividad mitótica muy alta, con hasta 16 figuras mitóticas por campo de alta potencia (Fig. 8). La IHQ con anticuerpo Ki-67 mostró un índice de proliferación Ki-67 muy alto, hasta del 56%, en correlación con la actividad mitótica elevada (Fig. 9). El origen glial del tumor se estableció por IHQ con el marcador glial GFAP que mostró una tinción fuerte y difusa del citoplasma de la célula tumoral (Fig. 10), mientras que un carcinoma de mama metastásico fue descartado por IHC con anticuerpos keratin CAM 5.2 y GCDFP-15. El anticuerpo p53 mostró una regulación positiva en algunos núcleos de células tumorales dispersos, lo que no sugiere una mutación TP53. Por el contrario, la IHQ con un anticuerpo específico para la mutación histona H3 K27M mostró una expresión fuerte y difusa de la proteína mutante en los núcleos de las células tumorales, pero no en los núcleos no tumorales de la vasculatura (Fig. 11). Este resultado estableció el diagnóstico final de este tumor como glioma difuso de línea media, mutante de histona H3 K27M (DMG/K27M), grado 4 de la OMS.
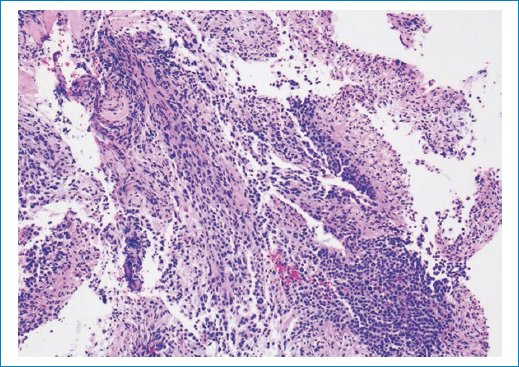
Figura 7. La tinción hematoxilina-eosina muestra infiltración difusa del neuropilo por una neoplasia hipercelular compuesta por pequeñas células azules con núcleos redondos hipercromáticos; focalmente, se observan células fibrilares con núcleos alargados. Aumento de la imagen: 10x.
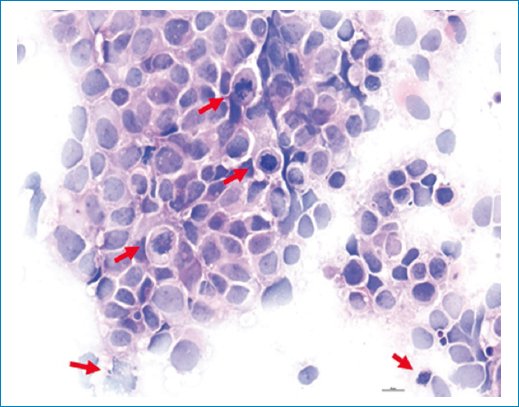
Figura 8. Aumento de la actividad mitótica. Preparación citológica intraoperatoria con hematoxilina y eosina que muestra frecuentes figuras mitóticas (flechas rojas). Imagen con aumento de 40x.
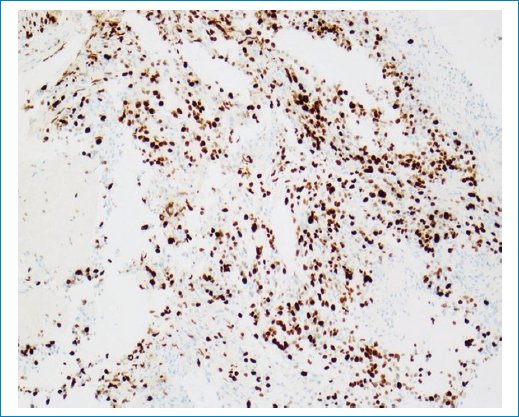
Figura 9. Índice de proliferación de Ki-67 muy alto. La inmunohistoquímica con anticuerpo Ki-67 muestra un índice de proliferación muy alto, en correlación con la alta actividad mitótica. Aumento de la imagen: 10x.
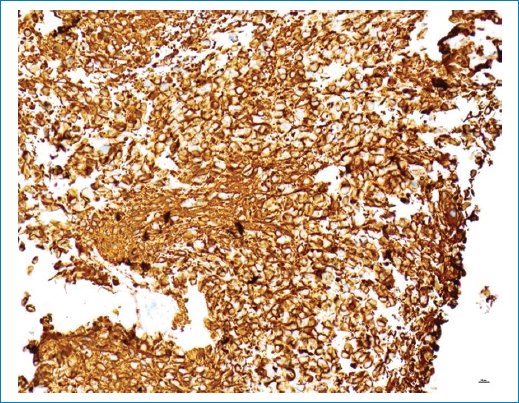
Figura 10. Origen glial. La inmunohistoquímica con anticuerpo GFAP, un marcador de tumores gliales, muestra una tinción citoplasmática intensa y difusa de las células tumorales. Aumento de la imagen: 20x. GFAP: proteína ácida fibrilar glial.
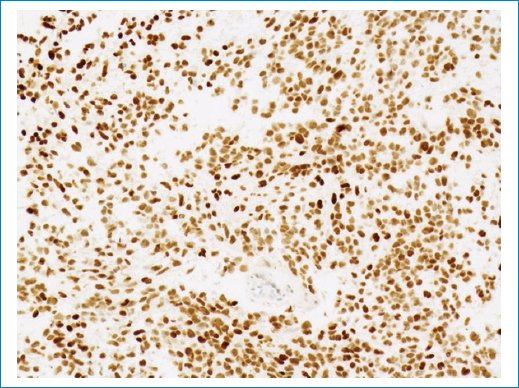
Figura 11. La mutación de la histona H3 K27M se detectó únicamente en las células tumorales. La presencia de la mutación se detectó mediante inmunohistoquímica con un anticuerpo específico para la mutación. Obsérvese la fuerte expresión nuclear en todas las células tumorales y la ausencia de expresión en las células vasculares no tumorales. Aumento de la imagen: 20x.
Análisis molecular
Se realizó un análisis genómico exhaustivo mediante secuenciación de nueva generación (NGS) de una biblioteca de 295 genes, como se describió previamente11,14. Este análisis confirmó la presencia de la mutación p.K27M de H3F3A, gen PPM1D, (que codifica la histona H3) en una fracción alélica variante, consistente con una mutación somática heterocigótica (Fig. 12). Se detectó una mutación patogénica en PPM1D p.W427* (protein phosphatase 1 D) en una fracción alélica variante en el rango de la línea germinal PPM1D. Aunque esta paciente no se sometió a pruebas genéticas, se demostró que esta mutación predispone al cáncer de mama en la base de datos ClinVar (https://www.ncbi.nlm.nih.gov/clinvar/). Cabe destacar que las mutaciones de PPM1D son relativamente frecuentes en DMG/K27M y se ha demostrado que son mutuamente excluyentes con las mutaciones de TP5310, como en este caso. También se detectaron dos mutaciones probablemente patógenas en el gen ATM (ataxia telangiectasia mutation) y, al igual que PPM1D, ATM es un gen implicado en la reparación del daño del ADN que a veces se inactiva en DMG/K27M (Diffuse Midline Glioma/H3 K27 Mutation)10.
También se realizó una prueba de metilación del promotor MGMT (O-6-methylguanine-DNA methyltransferase) para este tumor, la cual resultó negativa.
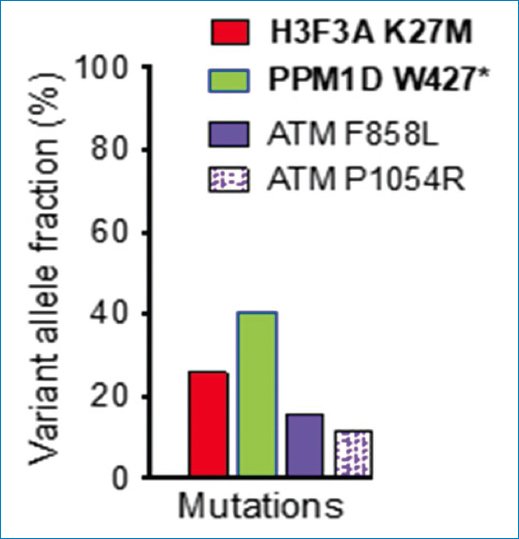
Figura 12. Análisis molecular. La secuenciación de nueva generación confirmó la presencia de la mutación p.K27M de H3F3A (que codifica la histona H3) en una fracción de alelos variantes, consistente con una mutación somática heterocigótica. También se detectaron una mutación p.W427* de mutación en el gen PPM1D, posiblemente patógena en la línea germinal, y dos mutaciones probablemente patógenas en el gen supresor tumoral ATM.
Conclusión
Hemos descripto las características de las imágenes de RM y anatomía patológica de un glioma medular difuso de la línea media, con alteración de tipo H3 K27. La RM sagital en STIR muestra una lesión intramedular expansiva con hiperintensidad difusa y longitudinalmente extensa, que excede el componente tumoral sólido, reflejando crecimiento infiltrativo y edema asociado. La histopatología corresponde a un glioma de médula espinal cervical de alto grado DMG/K27M en una paciente de 62 años con antecedentes de cáncer de mama. El análisis IHQ distinguió el glioma de alto grado de una metástasis de cáncer de mama, y el análisis molecular que detectó la mutación de la histona H3 K27M lo clasificó en la categoría relativamente nueva de la OMS de glioma difuso de línea media, mutante H3 K27M (DMG/K27M), grado 4 de la OMS. Se detectó una mutación adicional en el gen de reparación del daño al ADN PPM1D p.W427* y, basándose en su fracción alélica en el rango germinal, es posible que esta mutación predispusiera a ambas neoplasias malignas en esta paciente, lo que subraya la importancia del análisis molecular.
Financiamiento
Los autores declaran no haber recibido financiamiento para este estudio.
Conflicto de intereses
E. González-Toledo declara ser coeditor en jefe de la Revista Argentina de Radiología. M.M. Georgescu declara no tener conflicto de intereses.
Consideraciones éticas
Protección de personas y animales. Los autores declaran que los procedimientos seguidos se conformaron a las normas éticas del comité de experimentación humana responsable, de acuerdo con la Asociación Médica Mundial y la Declaración de Helsinki. Los procedimientos fueron autorizados por el Comité de Ética de la institución.
Confidencialidad, consentimiento informado y aprobación ética. Los autores han seguido los protocolos de su centro sanitario/institución para acceder a los datos de las historias clínicas. Se ha obtenido el consentimiento informado de la paciente y se cuenta con la aprobación del Comité de Ética. Se han seguido las recomendaciones de las guías SAGER.
Declaración sobre el uso de inteligencia artificial. Los autores declaran que no se utilizó ningún tipo de inteligencia artificial generativa para la redacción ni la creación de contenido de este manuscrito.